Der Artikel kompakt zusammengefasst
■ Um wasserseitige Korrosionsschäden an Eisenwerkstoffen durch Sauerstoffzutritt zu verhindern, muss der Zutritt von Sauerstoff in der Nutzungsphase minimiert und nicht zu verhindernde Einträge müssen möglichst weitgehend und sofort eliminiert werden.
■ Korrosionsschäden können auch an anderen metallenen Werkstoffen auftreten, wenn der pH-Wert nicht in deren passivem Bereich liegt, eine hohe Konzentration an Chloridionen oder auch viele sedimentierende Stoffe vorhanden sind.
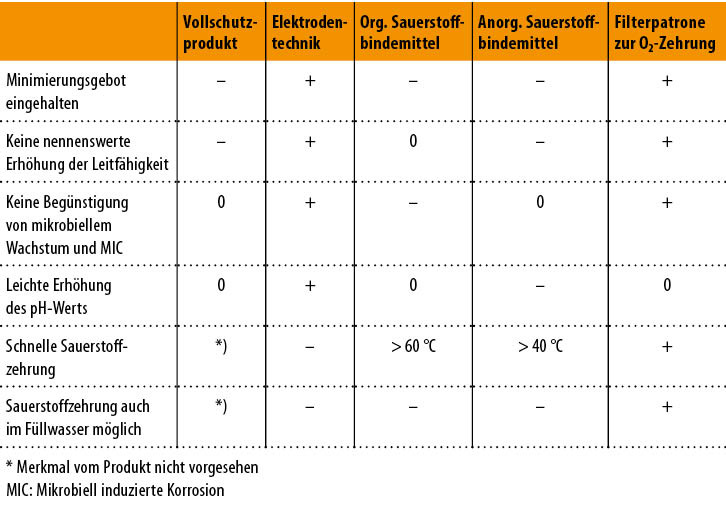
■ Vollschutzprodukte dienen nicht der Sauerstoffzehrung, sondern bewirken eine Schutzschichtbildung, sind aber kritisch zu bewerten. Chemische Verfahren können zwar Sauerstoff binden, aber mikrobiell induzierte Korrosionserscheinungen fördern.
■ Physikalisch-chemische Verfahren (Filterpatronen) können Sauerstoff zum größten Teil schon beim Befüllen und neu hinzutretenden Sauerstoff im Teilstrom während des Heizbetriebs zehren und zusätzlich das Umlaufwasser filtrieren.
Die in Deutschland bekannteste technische Regel zur Beurteilung der Korrosionsgefährdung von Heizanlagen ist VDI 2035 Blatt 2, eine aktualisierte Version liegt bereits im Entwurf [1] vor. Daneben gibt es noch DIN EN 14 868 [2] als Leitfaden für die Ermittlung der Korrosionswahrscheinlichkeit in geschlossenen Wasserzirkulationssystemen < 110 °C (also auch Kühl- und Kältesysteme), die es ebenfalls zu beachten gilt. Die Richtlinie VDI 2035 geht explizit von korrosionstechnisch geschlossenen Systemen aus, in denen es also keinen signifikanten Sauerstoffeintrag gibt, während DIN EN 14 868 zusätzlich auch Anlagen mit Sauerstoffzutritt in die Betrachtung einbezieht.
Die Rolle des Sauerstoffs
In den hier betrachteten Heiz- und Kühlsystemen werden die Korrosionsprozesse im Wesentlichen durch die Menge des eindringenden Sauerstoffs bestimmt – so lange sich der pH-Wert des Kreislaufwassers mehr oder weniger im Bereich von 8 bis 9 bewegt.
Grundsätzlich ist die Reduktion eines Oxidationsmittels (z. B. Sauerstoff) notwendig, damit der Auflösungsprozess am metallischen Werkstoff ungehindert weiter fortschreiten kann. Aber auch Säuren – erkennbar am niedrigen pH-Wert des Kreislaufwassers – erfüllen diese Voraussetzung. Die mögliche Geschwindigkeit dieses Korrosionsprozesses hängt aber noch von anderen Wasserparametern ab, dazu später mehr.
Sauerstoff kann auf verschiedenen Wegen in ein Heiz- oder Kühlsystem eingebracht werden,
- als gelöster Sauerstoff über das Füll- oder Ergänzungswasser (8 bis 11 mg/l),
- aus der Atmosphäre, durch partielle Unterdruckbildung im System (Entlüfter wird Belüfter!),
- durch direkten Kontakt des Wassers mit der Luft (offenes Ausdehnungsgefäß),
- mittels Diffusion durch organische Werkstoffe I (ältere Fußbodenheizsysteme ≠ DIN 4726),
- mittels Diffusion durch organische Werkstoffe II (Panzerschläuche bei T > 40 °C) und
- aus Luftpolstern, die bei Wartungs- oder Umbauarbeiten entstehen können.
Die Korrosionsrate bleibt vernachlässigbar gering, wenn der im Füllwasser vorhandene natürliche Sauerstoffgehalt durch Korrosionsprozesse verbraucht ist, über die Lebensdauer der Anlage nicht mehr als deren doppeltes Anlagenvolumen nachgespeist wird und Sauerstoffzutritt nicht nennenswert möglich ist. Bei großen, verzweigten Anlagen ist dies aber in der Praxis kaum zu realisieren.

perma-trade

perma-trade
Der Korrosionsprozess
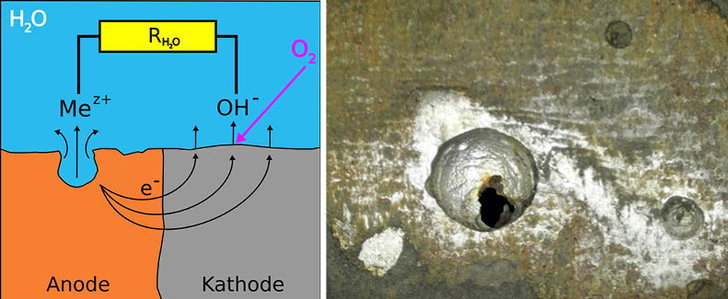
Grundsätzlich hat Schwarzstahl die Tendenz, sich in wässriger Umgebung (gemäß Fe e Fe2+ + 2 e–) aufzulösen, wie in (1) schematisch gezeigt. Die am Metall zurückbleibende Ladung (e–) wird in unmittelbarer Nähe zur Austrittstelle einem Oxidationsmittel – in der Regel im Wasser gelöstem Sauerstoff – angeboten, wobei sich Hydroxidionen gemäß ½ O2 + 2e– + H2O e 2 OH– bilden.
Der „elektrische“ Ladungsausgleich geht dabei über das Wasser und steht in direkter Beziehung zu dessen elektrischer Leitfähigkeit. Eine niedrige Leitfähigkeit (LF), wie sie bei salzarmer Betriebsweise gegeben ist, begrenzt die Korrosionsgeschwindigkeit deutlich, kann aber letztlich auch nicht vor Sauerstoffkorrosion schützen.
Werkstoffe aus Aluminiumlegierungen sind hinsichtlich Sauerstoffkorrosion deutlich weniger empfindlich, da sich dieser Werkstoff im sauerstoffhaltigen Wasser sehr gut passivieren kann. Sind allerdings Chloridionen in höherer Konzentration vorhanden, kann es trotzdem zu Lochkorrosion und Wanddurchbrüchen kommen. Dies gilt mehr oder weniger auch für molybdänfreie nichtrostende Stähle. Bei einer salzarmen Betriebsweise nach VDI 2035 (LF < 100 µS/cm) werden diese kritischen Chloridkonzentrationen jedoch nie erreicht.
Aber selbst, wenn für einen Werkstoff alle Wasserparameter passen, kann dieser trotzdem durch sedimentierende Stoffe, z. B. durch Korrosionsprodukte anderer Werkstoffe, so geschädigt werden, dass ein Schaden eintritt (2).
Wasserseitige Einflüsse auf die Sauerstoffkorrosion
Das Ausmaß sowie die Geschwindigkeit einer möglichen Sauerstoffkorrosionserscheinung hängen von mehreren Einflussfaktoren ab. Primärer Faktor ist die Konzentration an gelöstem Sauerstoff im Kreislaufwasser, aber auch die Parameter Härte, pH-Wert und Leitfähigkeit spielen eine Rolle. Dies soll nachfolgend etwas detaillierter beleuchtet werden.
Sauerstoffkonzentration
Nicht speziell entgastes oder sauerstoffgezehrtes Füllwasser enthält 8 bis 11 g/m3 gelösten Sauerstoff. Bei der Reaktion mit Bauteilen aus Schwarzstahl bildet sich dadurch letztlich Magnetit (je m3 Füllwasser ca. 36 g), gleichzeitig sinkt die Sauerstoffkonzentration auf Werte < 0,1 mg/l ab. In der Praxis werden bei korrosionstechnisch geschlossenen Anlagen Werte von 0,03 bis 0,1 mg/l gemessen. VDI 2035 nennt hier einen Grenzwert von 0,1 mg/l, unterhalb dessen keine Schäden zu erwarten sind. Für direkt an die Fernwärme angeschlossene Anlagen sind nach AGFW FW 510 aber strengere Vorgaben (0,02 – 0,1 mg/l) zu beachten.
Dem Korrosionsmodell von (1) entsprechend kann eine höhere Sauerstoffkonzentration auch mehr elektrische Ladung (e–) übernehmen, die von den austretenden positiven Eisenionen beim Übertritt ins Heizungswasser am Metall zurückgelassen werden. Diese Depolarisation stellt eine Voraussetzung für den ungehinderten Auflösungsvorgang des metallenen Festkörpers dar. Letztlich führt dies zu einem Versagen des Bauteils oder zumindest zu einer übermäßigen Bildung von Magnetit (3). Fehlt der Sauerstoff, kommt dieser Korrosionsprozess zum Stillstand.
Elektrische Leitfähigkeit des Heizungswassers
Beim Korrosionsvorgang nach (1) treten sowohl positive Fe2+- als auch negative OH–-Ionen in das Wasser über. Deren elektrischer Ladungsausgleich erfolgt über das Wasser und wird von einer zunehmenden Wasserleitfähigkeit begünstigt. Niedrige Leitfähigkeiten behindern neben diesem auch alle anderen elektrochemischen Vorgänge an der Metalloberfläche.
perma-trade
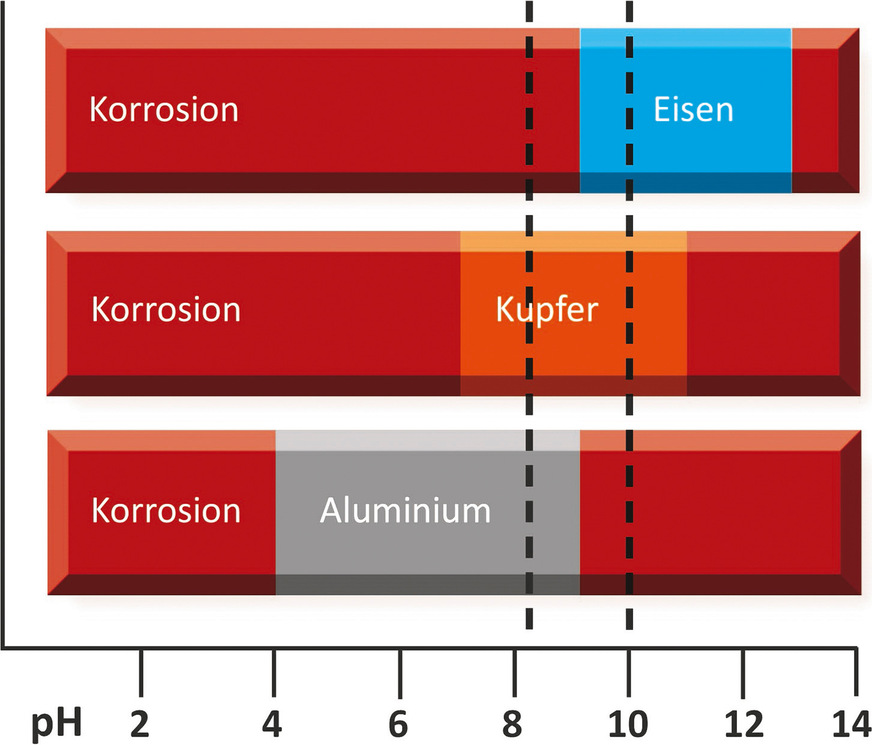
Die senkrechten Linien begrenzen den nach dem Stand der Technik (VDI 2035) einzuhaltenden Bereich
im Heizungswasser.
perma-trade
pH-Wert des Heizungswassers
Zunächst entscheidet der pH-Wert darüber, ob sich auf dem Metall eine Deckschicht ausbilden kann oder nicht. In (4) sind die pH-Wert-Bereiche für die Werkstoffe Eisen, Kupfer und Aluminium dargestellt, bei denen sich eine sogenannte Passivschicht aus Korrosionsprodukten bildet, die zumindest die weitere Flächenkorrosion massiv eindämmt.
Als bestmöglichen Kompromiss für die im Heizkreis verbauten Metalle fordern die einschlägigen Regelwerke, insbesondere VDI 2035, einen pH-Wert-Bereich von 8,2 – 9,0. Für Anlagen ohne Aluminiumkomponenten sollte der pH-Wert jedoch zwischen 9,3 und 10,0 gewählt werden, nicht nur wegen des dann passiven Verhaltens des Eisens, sondern auch, weil die Reduktion des Sauerstoffs an der Metalloberfläche vom pH-Wert abhängig ist und bei niedrigeren pH-Werten leichter abläuft.
Hinzu kommt noch, dass bei pH-Werten < 6,0 zunehmend die Säurekorrosion in Aktion tritt und die H+-Ionen den Sauerstoff als Oxidationsmittel abzulösen beginnen. Derart niedrige pH-Werte sind bei verschleppten, zu Säuren degradierten Frostschutzmittelresten im Heizungswasser keine Seltenheit.
Härte
Etwas Resthärte im Heizungswasser wirkt sich grundsätzlich positiv aus, was die Sauerstoffkorrosion betrifft. Dies rührt daher, dass die Reduktion von Sauerstoff die Metalloberfläche alkalisiert (Bildung von OH–, siehe oben), wodurch dort Kohlensäure gebunden wird. Befindet sich gelöster Kalk im Wasser, wird dieser sich an der alkalisierten Metalloberfläche abscheiden und so die weitere Reaktion behindern oder, mit anderen Worten: inhibieren.
Signifikant ist dieser Effekt vor allem bei neutralen Wässern. Korrosionschemisch betrachtet wirkt Kalziumkarbonat hier als sogenannter kathodischer Korrosionsinhibitor. Im Gegensatz zu anodisch wirkenden Inhibitoren kommt es hierbei zu keiner erhöhten
lokalen Korrosionserscheinung bei einer Unterdosierung.
In der Zusammenfassung bedeutet dies, dass eine salzarme Betriebsweise mit möglichst hohem pH-Wert wasserseitig zwar den bestmöglichen Korrosionsschutz darstellt, aber für die Fälle eines nennenswerten Sauerstoffeintrags keinen wirklichen Schutz bietet. Lässt sich ein Sauerstoffeintrag nicht durch andere technische Maßnahmen, z. B. eine Systemtrennung, beherrschen, können die direkte Sauerstoffbindung oder auch der Einsatz von Korrosionsinhibitoren im Heizwasser erwogen werden.
Bevor die Möglichkeiten der Sauerstoffbindung beleuchtet werden, sind noch Hinweise zu Vollschutzprodukten, die auch in korrosionstechnisch offenen Systemen zum Einsatz kommen, angezeigt.
Vollschutzprodukte
Vollschutzprodukte enthalten meist auch anodisch wirkende Korrosionsinhibitoren, die in der Wirkstoffkonzentration – i. d. R. jährlich – zwingend überprüft werden müssen und mehr oder weniger nur auf blanken Metalloberflächen messtechnisch schöne Ergebnisse von Schutzschichten zeigen. Deshalb wird auch eine vorhergehende, chemische Reinigung vom Hersteller gefordert.
Benzotriazole, eine häufig verwendete Substanzgruppe, zeigen eine hohe Mobilität im Boden, werden von der Kläranlage nur unzureichend entfernt und gelangen so in die aquatische Umwelt (Grundwasserdatenbank Wasserversorgung, 23. Jahresbericht 2014). Gilt das Produkt als biologisch abbaubar, dient es nebenbei noch als Nahrung für Mikroorganismen, die nicht nur isolierende Biofilme bilden, sondern unter Umständen Sulfat zu stark korrosiv wirkendem Sulfid reduzieren können. Dem wiederum wird oft mit einem Biozidzusatz begegnet. Das Minimierungsgebot wird hierbei komplett übergangen.
Elektrochemische Verfahren zur Sauerstoffbindung
Elektrochemische Verfahren zur Sauerstoffbindung nutzen ein „unedles“ Metall – in der Regel eine Magnesiumlegierung – im galvanischen Kurzschluss mit einem Bauteil aus Edelstahl. Während sich das Magnesium auflöst, findet parallel dazu an der Edelstahloberfläche die elektrochemische Reduktion von Sauerstoff statt. In der Summe entsteht dann Magnesiumhydroxid als Korrosionsprodukt, das als Schlamm entfernt werden muss. Gleichzeitig wird der pH-Wert etwas angehoben.
So weit, so gut, wäre dabei nicht die Sauerstoffbindegeschwindigkeit recht niedrig und das Gerät auch eher für den Hauptstrom auszulegen. Wird die Anlage salzarm betrieben, ist der Einsatz zu hinterfragen. Entgegen anderslautenden Aussagen empfiehlt VDI 2035 den Einsatz dieser Geräte nicht explizit als technisch gute Lösung zur Sauerstoffbindung.
perma-trade
Chemische Verfahren zur Sauerstoffbindung
Für die chemische Bindung von Sauerstoff wird meist Natriumsulfit dosiert, das ab Temperaturen von ca. 40 °C eine hohe Sauerstoffbindegeschwindigkeit zeigt. Organische Bindemittel wirken erst oberhalb von 60 °C, fördern die Biofilmbildung und erhöhen so die Wahrscheinlichkeit für mikrobiell induzierte Korrosionserscheinungen (MIC). VDI 2035 rät deshalb – in ihrem Gültigkeitsbereich – zum Verzicht.
Auch Natriumsulfit zeigt Nebenwirkungen. Bei der Reaktion mit Sauerstoff entsteht Sulfat, das die Leitfähigkeit des Heizungswassers im Laufe der Zeit stark erhöht. In der Anlagenpraxis finden sich hier nicht selten Werte bis 2000 µS/cm, was gelegentlich Ausblühungen (Salzkrusten) an Regelventilen verursacht. Zudem besteht vor allem im Niedertemperaturbereich auch wieder eine erhöhte Wahrscheinlichkeit, dass sulfatreduzierende Mikroorganismen korrosiv wirkendes Sulfid erzeugen.
Physikalisch-chemisches Verfahren
Beim neuen physikalisch-chemischen Verfahren (Filterpatrone) kann der im Wasser gelöste Sauerstoff direkt beim Hindurchströmen eliminiert werden. Der Prozess ist allerdings von der Wassertemperatur abhängig. Wird eine Heizanlage mit kaltem Wasser über eine solche Patrone – ggf. in Kombination mit einer Entsalzung oder Enthärtung – neu befüllt, können dem Füllwasser direkt 80 % Sauerstoff entzogen werden. In der Folge bilden sich dann auch 80 % weniger Korrosionsprodukte, die beispielsweise Topmeter von Fußbodenheizungsverteilern belegen könnten. Dabei ist es unerheblich, ob die Sauerstoffzehrpatrone vor oder hinter der Aufbereitungseinheit platziert wird.
Prädestiniert für dieses Filterverfahren ist die Anwendung während des Heizbetriebs im Teilstrom, wobei bereits ab einer Wassertemperatur von 40 °C der Sauerstoff mit hoher Geschwindigkeit auf eine Restkonzentration von < 0,02 mg/l gezehrt wird. Im einfachsten Fall kann mittels Edelstahlwellrohren und einem Tacosetter eine solche Filterpatrone zwischen Rücklauf und Vorlauf (saugseitig!) installiert werden.
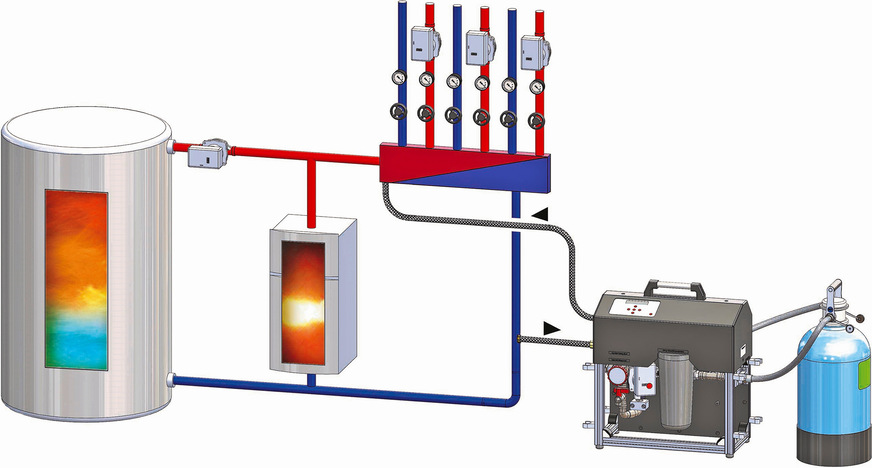
Technisch eleganter ist die Lösung in Kombination mit einem festinstallierten Modul zur Teilstromentsalzung (5). Hier kann das Wasser entweder ständig oder zeitgesteuert mechanisch filtriert und vom Restsauerstoff befreit werden. Falls erforderlich, lässt sich zudem
eine Entsalzungspatrone in Abhängigkeit der Leitfähigkeit des Anlagenwassers automatisch hinzuschalten.
Literatur
[1] VDI 2035 Blatt 1 (Entwurf) Vermeidung von Schäden in Warmwasser-Heizungsanlagen, Steinbildung und wasserseitige Korrosion. Berlin: Beuth Verlag, März 2019
[2] DIN EN 14 868 Korrosionsschutz metallischer Werkstoffe – Leitfaden für die Ermittlung der Korrosionswahrscheinlichkeit in geschlossenen Wasser-Zirkulationssystemen. Berlin: Beuth Verlag, November 2005
[3] Kruse, C.-L.: Der Lufteintrag ist nach wie vor ein Problem. Winnenden: Heizungs-Journal Verlag, Heizungsjournal 12-2008
[4] BDH Informationsblatt Nr. 3 – Korrosionsschäden durch Sauerstoff im Heizungswasser – Sauerstoffkorrosion. Köln: Bundesverband der Deutschen Heizungsindustrie, März 03-2011
[5] Ende, D.: Heizungswasseraufbereitung ohne Betriebsunterbrechung. Winnenden: Heizungs-Journal Verlag, Heizungsjournal 06-2015

Bild: perma-trade
Sauerstoffmessung im Heizungswasser
Um es gleich vorweg zu nehmen: Das Heizwasser muss direkt beim Ausströmen an der Anlage bei einer Temperatur < 50 °C gemessen werden. Eine Probennahme für ein Labor oder die Messung in einem Gefäß bringt falsche, deutlich zu hohe Werte. Auch sollte vorzugsweise eine optische Messsonde eingesetzt werden, da diese schnell anspricht und mit sehr niedrigen Sauerstoffkonzentrationen zurechtkommt. Vorgehensweise:
- Stagnationswasser an der Probennahmestelle verwerfen.
- Trichter mit Schlauchstück anbringen (Tülle am KFE-Hahn oder am Probennahmekühler) und
- Wasser über Trichter ausströmen lassen, dabei Messsonde tief eintauchen.
- Die Sonde sollte mit ca. 0,3 m/s (ca. 2 l/Min) bei T < 50 °C angeströmt werden.
- Wird die Temperatur konstant angezeigt, kann der Messwert abgelesen werden.
Die Messung der gelösten Sauerstoffkonzentration gibt zwar eine wichtige Auskunft, ist aber mehr oder weniger eine Momentaufnahme und hängt oft noch vom Messort in der Anlage ab. Korrespondierend zum aktuellen Entwurf für VDI 2035 Blatt 1 sollte die Konzentration des gelösten Sauerstoffs < 0,1 mg/l sein (Richtwert), damit die Korrosionswahrscheinlichkeit für die in Fließrichtung nachfolgenden Bauteile gering bleibt.